viernes, 7 de junio de 2013
viernes, 31 de mayo de 2013
ELECTROLISIS del H2O
Materiales:
1. Un
vaso de precipitación de 500ml
2. 2
tubos de ensayo
3. Un
cargador de celular con dos cables cocodrilo
4. Electricidad(
en chufe)
5. 2
lápices
6. Un
pedazo de cartón
Reactivos:
1.
Solución salina (agua + sal )
2.
Sulfuro de cobre
PROCEDIMIENTO:
·
En un vaso de precipitación poner sulfuro de
cobre, y disolverlo con agua destilada de tal manera que no queden pequeñas
bolitas en el fondo. Conectar el cargador previamente sacados los cables,
realizar un circulo en el cartón más
grande que el vaso de precipitación, realizar dos orificios en el mismo
de tal manera que entren los lápices (sacados punta de los dos lados) y queden
dentro del vaso de precipitación; al un extremo vamos a colocar los cables de
tal manera que la otra punta quede dentro de la solución.
·
En un vaso de precipitación con solución salina.
Conectar el cargador previamente sacados los cables, realizar un circulo en el
cartón más grande que el vaso de
precipitación, realizar dos orificios en el mismo de tal manera que entren los
lápices (sacados punta de los dos lados) y queden dentro del vaso de precipitación;
al un extremo vamos a colocar los cables de tal manera que la otra punta quede
dentro de la solución.
·
En un recipiente vamos a colocar solución
salina, en los dos tubos de ensayo vamos a encajar, correspondientemente los
cables de tal manera que no se salgan, los vamos a colocar dentro del agua.
·
En un recipiente con solución salina vamos a
colocar dentro de los dos tubos de ensayo, lápices y al igual que el primer
procedimiento vamos a colocar dentro de los tubos de ensayo los lápices,
correspondientemente con los cables apresados de un lado e introducimos en la
solución.
CONCLUSIONES:
viernes, 24 de mayo de 2013
MISCIBLE O IN MISCIBLE
Experimento nº 3
NATURALEZA
DEL SOLUTO
v
Limpiar y secar tres tubos de ensayo y colocar
1cm3 de tetracloruro de carbono.
v
En cada uno de ellos añadir pequeñas porciones
de azúcar, cloruro de sodio, aceite.
v
Trata de disolver cada sustancia por agitación.
Experimento nº4
NATURALEZA DEL SOLUTO Y DEL
SOLVENTE
o En
6 tubos de ensayo colocar 5cm3 de agua
o Añadir
a cada tubo respectivamente pequeñas porciones de carbono de calcio, cloruro de
sodio, sulfato cúprico, 10 gotas de tetracloruro de carbono, 10 gotas de
aceite, 10 gotas de acido clorhídrico.
o Agitar
y dejarlos reposar por un tiempo de 3 minutos.
CUADRO COMPARATIVO
esto nos ayudara a entender mas acerca del tema
esto nos ayudara a entender mas acerca del tema
|
Carbonato de calcio
|
soluble
|
miscible
|
|
Cloruro de sodio
|
Soluble
|
inmiscible
|
|
Sulfato cúprico
|
Insoluble
|
inmiscible
|
|
Tetracloruro de carbono
|
Insoluble
|
inmiscible
|
|
Aceite
|
Insoluble
|
inmiscible
|
|
Acido clorhidrico
|
soluble
|
miscible
|
viernes, 17 de mayo de 2013
SOLUBILIDAD
Materiales:
1. Lámpara
de alcohol
2. Tubos
de ensayo
3. Pinza
para tubos de ensayo
4. gradilla
5. dicromato
de potasio
6. azúcar
7. cloruro
de sodio
8. carbonato
de calcio
9. sulfato
cúprico
10. tetracloruro
de carbono
11. aceite
12. ácido
clorhídrico
13. agua
PROCEDIMIENTO:
Experimento nº
1
EFECTOS DE LA AGITACIÓN, TAMAÑO DEL GRANO
Y TEMPERATURA SOBRE LA SOLUBILIDAD
·
Dividir una porción aproximada de 0.5 de
dicromato de potasio y pulverizarla
·
Introducir el dicromato de potasio en un tubo de
ensayo que contenga 5cm3 de H2O
·
A continuación agitar el tubo de ensayo y
someterlo al calor sin que llegue a la ebullición y observar lo que sucede.
Experimento
nº2
NATURALEZA DEL SOLVENTE
§ Colocar
en un tubo de ensayo agua hasta la mitad y 2cm3
§ En
otro tubo de ensayo colocar 2cm3 de tetracloruro de carbono (el tubo de ensayo
debe estar perfectamente seco)
§ Colocar
una pequeña cantidad de yodo en ambos tubos (las porciones de yodo deben ser
iguales )
nNota : podremos diferenciar que no todos los compuestos son solubles y que a partir de la ebullición muchos de estos pueden disolverse, como coagularse. Es importante tener en cuenta que hay que tener cuidado al manejar los reactivos
viernes, 10 de mayo de 2013
Tipificacion Sanguinea
Es un método para decirle cuál es el tipo específico de sangre que usted tiene. El tipo de sangre que usted tenga depende de si hay o no ciertas proteínas, llamadas antígenos, en sus glóbulos rojos.
La sangre a menudo se clasifica de acuerdo con el sistema de tipificación ABO. Este método separa los tipos de sangre en cuatro categorías:
- Tipo A
- Tipo B
- Tipo AB
- Tipo O
Su tipo de sangre (o grupo sanguíneo) depende de los tipos que haya heredado de sus padres.
MATERIALES :
* 1 torunda con alcohol
* 1 lanceta esteril (yo usaba agujas de las jeringas porque es mucho más cómodo y mucho menos doloroso)
reactivos Anti-A, Anti-B y Anti-D( que es para el factor rhesus)
* 1 bandita para poner en el dedo al final de tomar la muestra de sangre
* 1 portaobjetos
* 1 palillo de madera(para mezclar la sangre con el reactivo)
*De preferencia usar guantes de látex aunque no interfiere en nada por la sencilla prueba
* 1 lanceta esteril (yo usaba agujas de las jeringas porque es mucho más cómodo y mucho menos doloroso)
reactivos Anti-A, Anti-B y Anti-D( que es para el factor rhesus)
* 1 bandita para poner en el dedo al final de tomar la muestra de sangre
* 1 portaobjetos
* 1 palillo de madera(para mezclar la sangre con el reactivo)
*De preferencia usar guantes de látex aunque no interfiere en nada por la sencilla prueba
COMO REALIZARLO :
bueno primero que nada le pides al paciente que se ponga cómodo, luego se procede a explicar de qué trata la prueba, simple y sencillamente es una toma de sangre del dedo o del lóbulo de la oreja y por medio de aglutinación se obtiene el resultado.
Entonces tomas la mano del paciente(es muy regular en la mano) y le tomas el dedo índice o pulgar (prefiero el índice, es mucho mejor q el pulgar), y vas dándole masajes y apretándolo para que haya mucha irrigación sanguínea, entonces destapas la lanceta o la jeringa frente al paciente y le dices q es nuevo, y de allí procedes a tomar de nuevo el dedo del paciente y ahora lo mantienes apretado para q la sangre se concentre en el lugar, con la torunda húmeda por el alcohol procedes a limpiar la zona, secas y entonces procedes a dar el piquete para obtener la sangre.
Una vez que hayas obtenido una gota de sangre, procedes a depositar 3 gotas en un portaobjetos de vidrio, secas el dedo del paciente con otra torunda y le aplicas la banda.
Entonces a cada gota de sangre le aplicas 1 gota de reactivo, a la primera le pones una gota de Anti-A, a la segunda una de Anti-B y a la tercera una de Anti-D, entonces con el palillo de madera lo mezclas bien bien y entonces le das pequeños giros para q se mezcle bien bien y haya aglutinaciones o no.
bueno primero que nada le pides al paciente que se ponga cómodo, luego se procede a explicar de qué trata la prueba, simple y sencillamente es una toma de sangre del dedo o del lóbulo de la oreja y por medio de aglutinación se obtiene el resultado.
Entonces tomas la mano del paciente(es muy regular en la mano) y le tomas el dedo índice o pulgar (prefiero el índice, es mucho mejor q el pulgar), y vas dándole masajes y apretándolo para que haya mucha irrigación sanguínea, entonces destapas la lanceta o la jeringa frente al paciente y le dices q es nuevo, y de allí procedes a tomar de nuevo el dedo del paciente y ahora lo mantienes apretado para q la sangre se concentre en el lugar, con la torunda húmeda por el alcohol procedes a limpiar la zona, secas y entonces procedes a dar el piquete para obtener la sangre.
Una vez que hayas obtenido una gota de sangre, procedes a depositar 3 gotas en un portaobjetos de vidrio, secas el dedo del paciente con otra torunda y le aplicas la banda.
Entonces a cada gota de sangre le aplicas 1 gota de reactivo, a la primera le pones una gota de Anti-A, a la segunda una de Anti-B y a la tercera una de Anti-D, entonces con el palillo de madera lo mezclas bien bien y entonces le das pequeños giros para q se mezcle bien bien y haya aglutinaciones o no.
RESULTADOS DE LA AGLUTACION:
A POSITIVO: AGLUTINA ANTI-A Y ANTI-D
A NEGATIVO: AGLUTINA ANTI-A PERO ANTI-D NO
B POSITIVO: AGLUTINA ANTI-B Y ANTI-D
B NEGATIVO: AGLUTINA ANTI-B PERO ANTI-D NO
AB POSITIVO: AGLUTINAN LAS 3 GOTAS
AB NEGATIVO: AGLUTINA ANTIA- ANTI-B PERO ANTI-D NO
O POSITIVO: AGLUTINA SOLO ANTI-D
O NEGATIVO: NO EXISTE AGLUTINACION
De alli diferenciamos al donador universal que es el O negativo, porque no tiene proteínas q puedan ser detectadas y combatidas por la respuesta inmune
y al receptor universal que es el AB positivo, que tiene todas las proteínas posibles y puede recibir de cualquier otro sin que la respuesta inmune por rechazo se active.
A POSITIVO: AGLUTINA ANTI-A Y ANTI-D
A NEGATIVO: AGLUTINA ANTI-A PERO ANTI-D NO
B POSITIVO: AGLUTINA ANTI-B Y ANTI-D
B NEGATIVO: AGLUTINA ANTI-B PERO ANTI-D NO
AB POSITIVO: AGLUTINAN LAS 3 GOTAS
AB NEGATIVO: AGLUTINA ANTIA- ANTI-B PERO ANTI-D NO
O POSITIVO: AGLUTINA SOLO ANTI-D
O NEGATIVO: NO EXISTE AGLUTINACION
De alli diferenciamos al donador universal que es el O negativo, porque no tiene proteínas q puedan ser detectadas y combatidas por la respuesta inmune
y al receptor universal que es el AB positivo, que tiene todas las proteínas posibles y puede recibir de cualquier otro sin que la respuesta inmune por rechazo se active.
viernes, 26 de abril de 2013
experimento de rutherford
La importancia histórica del experimento de Rutherford fue enorme. No solo demostró la incorrección de la propuesta de Thomson Al sugerir poderosamente la idea de un modelo de átomo planetario, generó una contradicción insalvable entre la mecánica newtoniana y el electromagnetismo que fue la puerta de entrada de de la incipiente teoría cuántica en el universo del átomo.En nuestra práctica docente hemos constatado que tras explicar el experimento de Rutherford los alumnos acaban adquiriendo la siguiente idea:El experimento de Rutherford demuestra que el modelo de Thomson no es válido porque la mayoría de las partículas alfa atraviesan la lámina de oro y solo unas pocas rebotan.Este error de apreciación (lo que demuestra la incorrección del modelo de Thomson es el hecho de que algunas partículas alfa rebotan) no se puede despreciar, ya que conduce a pensar que la predicción del modelo de Thomson para el experimento de Rutherford es que la mayoría de las partículas alfa rebotan (la predicción del modelo de Thomson es precisamente la contraria: ninguna partícula rebota).El problema radica en que nuestros alumnos tienen la idea previa de que las partículas alfa, cuando choquen con cualquier cosa, deben rebotar (presuposición de impenetrabilidad de la materia). Es por ello, que lo que les sorprende del experimento de Rutherford no es que haya partículas que reboten, sino que las partículas atraviesen la lámina de oro.Por esta razón consideramos que, antes de abordar el experimento de Rutherford, es necesario que los alumnos adquieran cierto conocimiento intuitivo de como predicen las simulaciones que se comportan las partículas alfa al incidir sobre diferentes tipos de distribuciones de carga. En este contexto es importante conseguir superar la presuposición de impenetrabilidad de la materia.Una vez clarificada cual es la predicción del modelo de Thomson se puede realizar el experimento de Rutherford de forma cualitativa y analizar los resultados que se obtienen. El objetivo es que el conocimiento adquirido por los alumnos les permita identificar correctamente cual es la distribución de carga responsable de aquello que observan.La idea que proponemos es poner a los alumnos "en situación" para que el resultado experimental que obtienen "les sorprenda" por como contradice el modelo de Thomson. Solo después creemos conveniente la utilización de simulaciones o animaciones en las que se muestre simultáneamente el modeló de átomo nuclear y su respuesta de dispersión cuando es bombardeado por el haz de partículas alfa.Así pues, para el estudio del experimento de Rutherford planteamos la realización de tres actividades. A continuación abordamos el desarrollo de las mismas en detalle1. Estudio de la dispersión de partículas por diferentes distribuciones de carga.2. Realización del experimento de Rutherford y análisis de resultados.3. Visualización simultánea del modelo de átomo nuclear y su respuesta frente al bombardeo de partículas alfa.
viernes, 19 de abril de 2013
EXPERIMENTO DE TORRICELLI
EVANGELISTA TORRICELLI, nació en 1608 hasta 1647 fue un físico, matemático italiano y discípulo de Galileo. Fue el primero (en 1643) que logró medir la presión atmosférica mediante un curioso experimento.
El experimento, realizado en un laboratorio 1643, consistía en medir la PRESIÓN ADMOSFERICAMENTE este proceso:
Torricelli llenó de mercurio un tubo de 1 m de largo, (cerrado por uno de los extremos) y lo invirtió sobre una cubeta llena de mercurio, de inmediato la columna de mercurio bajó varios centímetros, permaneciendo estática a unos 76 cm (760 mm) de altura ya que en esta influía la presión atmosférica.
Como según se observa la presión era directamente proporcional a la altura de la columna de mercurio (h), se adoptó como medida de la presión el mm (milímetro) de mercurio.
Así la presión considerada como "normal" se correspondía con una columna de altura 760 mm.
La presión atmosférica se puede medir también en atmósferas (atm):
1 atm=760 mm=101.325 Pa =1,0 “kilo” (kgf/cm2)
Torricelli llegó a la conclusión de que la columna de mercurio no caía debido a que la presión atmosférica ejercida sobre la superficie del mercurio (y transmitida a todo el líquido y en todas direcciones) era capaz de equilibrar la presión ejercida por su peso.
1 mbar o hPa = 0,7502467 mmHg
Torricelli tambien aporto a el principio de pascal
viernes, 12 de abril de 2013
BURBUJAS DE FUEGO
MATERIALES :
AEROSOL
JABÓN LIQUIDO
UN RECIPIENTE
AGUA
PROCEDIMIENTO:
en agua previamente disuelta con el jabón , vamos a introducir el aerosol provocando que se hagan burbujas de tal manera que al encender el mismo vamos a tener las burbujas inflamables.
RECOMENDACIÓN:
Mantenerse alejado de el mismo a los niños, tener cuidado y prevenir con una franela mojada.
AEROSOL
JABÓN LIQUIDO
UN RECIPIENTE
AGUA
PROCEDIMIENTO:
en agua previamente disuelta con el jabón , vamos a introducir el aerosol provocando que se hagan burbujas de tal manera que al encender el mismo vamos a tener las burbujas inflamables.
RECOMENDACIÓN:
Mantenerse alejado de el mismo a los niños, tener cuidado y prevenir con una franela mojada.
viernes, 5 de abril de 2013
Llamarada de fuego

materiales
harina
velas
plato
sorbete
procedimiento:
con la harina en un plato y el sorbete vamos a parar en frente tuyo las velas encendidas , de tal manera que vamos a soplar y vamos a ver las llamaradas de fuego.
lo podemos observar en la siguiente pagina.-
http://www.youtube.com/watch?v=qwNoH3cfVRE
lunes, 1 de abril de 2013
Materiales:
Pastillas de cloruro de potasio
Azúcar
Las pastillas de cloruro de potasio se venden en las farmacias. El azúcar, conviene que sea Impalpable, que es esa que viene molida como polvo. Si bien tiene un poco de almidón, no interferirá con el experimento.
Procedimiento:
Lo primero que tienes que hacer es moler las pastillas de cloruro de potasio hasta dejarlas como un fino polvo. Para ello, coloca un papel sobre la mesa, pones las pastillas sobre el papel, y las presionas con una cuchara. Haces eso hasta que sólo quede polvo. Para terminar con el cloruro, cuenta cuantas cucharadas de polvo has creado.
viernes, 29 de marzo de 2013
HIELO SECO
 EXPERIMENTOS CON HIELO SECO
EXPERIMENTOS CON HIELO SECO
Antes de comenzar a realizar experimentos con hielo seco, debemos comprender qué es este material y cuáles son las propiedades que lo vuelven muy peligroso si no se utiliza responsablemente.
El hielo seco es dioxido de carbono en estado sólido, y su principal característica es que pasa del estado sólido al gaseoso directamente, lo que proporciona un aumento de volumen tal que si se lo contiene en un envase cerrado el mismo estallará debido a la fuerte presión que le ejercerá el gas.
Se pueden conseguir algunos trozos pequeños para experimentar principalmente en las heladerías, aunque existen muchas empresas que lo proveen de manera industrial.
MATERIALES:
HIELO SECO
AGUA
JABÓN LIQUIDO
UNA TOALLA TERESITA
PROCEDIMIENTO:
En un envase diluir agua con jabón de tal manera que vamos a introducir la teresita, después en otro envase vamos a colocar hielo seco con un poco de agua vamos a poner al rededor con la toalla mojada cubriendo sus lados; de tal manera que se formara una burbuja de hielo seco, al llenar de gas esta va a salir o explotar sola.
viernes, 22 de marzo de 2013
Alimentando bacterias
Materiales:
- Un pequeño plato de agar
- Bastoncillos de algodón
- Recipiente con tapa
- Periódicos viejos
viernes, 15 de marzo de 2013
LIPIDOS
MATERIALES:
Albumina
Tubos de ensayo
solucion de NAOH
FELING A
Coloración violeta rosácea característica con el sulfato de
cobre (II) en medio básico. Es
la reacción de Biuret y se debe a los enlaces peptídicos que
unen los aminoácidos, los
cuales en presencia de un álcali forman el llamado complejo
de biuret que al reaccionar
PASOS:
con el sulfato cúprico da la coloración violeta.
1. Pon unos 3 ml de disolución de albúmina en un tubo de
ensayo.
2. Añade 3 ml de solución de NaOH.
3. Añade unas gotas de Licor de Fehling A (que es sulfato de
cobre).
4. Agita y observa el resultado
Puedes utilizar para el experimento clara de huevo diluida
en un poco de agua.
martes, 12 de marzo de 2013
Tinta invisible
1.- Escribir el mensaje en una hoja de papel blanco con leche o jugo de limón, usando una pluma o un palito de madera con punta como lapicera (conviene usar trazos gruesos), y dejar secar. El mensaje puede revelarse calentando la hoja de papel con una plancha bien caliente o en el horno de la cocina (con el permiso de su dueña…).
2.- Escribir de la misma forma con una solución de almidón, preparada mezclando una cucharadita de almidón de maíz (maicena) o de trigo con 1/4 taza de agua, calentando hasta ebullición y dejando enfriar. El mensaje se revela mojando la hoja de papel con una solución diluída de yodo, que se prepara agregando varias gotas de tintura de yodo (que se compra en la farmacia) a 1/4 taza de agua. El escrito aparece en color azul sobre un fondo celeste.
Y ya que estamos, probemos de agregar una gota de tintura de yodo a varios mililitros de solución de almidón, agitando el recipiente después. El color azul obscuro, casi negro, que aparece explica el “funcionamiento” de la tinta invisible que describimos y es una manera que usan los químicos para detectar la presencia de pequeñísimas cantidades de yodo.
Es ácido o alcalino?
El agua pura no es ni ácida ni alcalina. Es neutra. Pero cuando se disuelven cosas en agua, se obtienen soluciones que probablemente ya no sean neutras. Serán ácidas, como el vinagre, el jugo de limón, etc., o alcalinas (también denominadas básicas), como el agua de cal, algunos jabones, algunos líquidos limpiadores de uso doméstico, etc.
Para determinar si una solución es ácida o alcalina, los químicos usan sustancias llamadas indicadores, que cambian de color según como sea la solución que se estudia. Mamá Naturaleza nos ofrece algunos de esos indicadores en la forma de los colorantes de las flores y otros vegetales (esos colorantes se llaman antocianinas).
Otra posibilidad es hervir el vegetal con agua durante unos 10 minutos y dejar enfriar, o simplemente molerlo con un poco de agua (en una licuadora, por ejemplo). Las soluciones en agua suelen ser algo turbias, a diferencia de los extractos con alcohol.Veamos como se prepara fácilmente una solución de indicador. Necesitaremos algunas campanillas azules, esas flores de las enredaderas que crecen en muchos terrenos baldíos y que se muestra en la figura. También pueden servir algunas hojas de repollo colorado. Tomamos esas flores u hojas, las convertimos en tiras finas con un cuchillo, las colocamos en un vaso y las cubrimos con un poco de alcohol fino.
Luego de filtrar el líquido obtenido a través de un trozo de tela o algodón, o de un papel de filtro para café, tendremos listo nuestro indicador, con un hermoso color azul.
Pongamos un poco del indicador en dos vasos y agreguemos a uno, unas gotas de vinagre (ácido): el líquido tomará color rojo; al otro, unas gotas de limpiador desengrasante para cocina o de amoníaco (álcali): el indicador tomará color verde. Tendremos entonces:
Solución de indicador + ácido: color rojo
Solución de indicador (neutro): color azul
Solución de indicador + álcali: color verde
Pero esas reacciones pueden invertirse. Si a la solución ácida de color rojo le agregamos un poco de solución alcalina (como limpiador desengrasante) el color virará a verde, pasando por azul. O sea que la solución ácida es neutralizada por el álcali, y finalmente se vuelve alcalina.
También podemos neutralizar la solución alcalina de color verde agregándole vinagre: tomará color azul, y finalmente color rojo, si se agrega un exceso de ácido.
Es una buena idea experimentar con colorantes de distintos vegetales (flores, remolacha, etc.) para prepara el indicador…
Y teniendo un indicador que funciona bien, intentemos determinar si los distintos líquidos que encontramos en nuestra casa o nuestro cuerpo son ácidos o alcalinos…
Otro indicador: Podemos preparar fácilmente un indicador comprando un chicle laxante (conteniendo fenolftaleina) en la farmacia y agitándolo en un vaso con un poco de agua. Luego filtrar para obtener una solución límpida. La solución así obtenida será incolora en medio ácido o neutro y tomará color rosado violáceo en medio alcalino.
De metales y pilas.
Los metales tienen cierta tendencia a disolverse en el agua, unos más, otros menos. Si sumergimos una chapa de cinc en agua, algunos átomos de cinc perderán dos electrones (o sea, dos cargas negativas) y se convertirán en iones (cinc)++, con dos cargas positivas. Sin embargo, esos iones se quedan “pegados” al metal, porque no quieren alejarse de los electrones (cargas de distinto signo se atraen!). Pero si hay algo que se lleve los electrones, entonces si que esos iones (cinc)++ pasarán a la solución!
Probemos el siguiente experimento:
Preparamos una solución de sulfato de cobre, como la mencionada en el experimento de los cristales (se puede preparar en frío y no hace falta que sea saturada). Ahora tomamos un trozo de alambre galvanizado bien limpio y lo sumergimos en la solución. Veremos que el alambre queda cubierto por una capa de cobre de color rojizo. Qué pasó?
La solución azul que usamos debe su color a los iones (cobre)++. Cuando sumergimos el alambre galvanizado (que es de hierro recubierto de cinc metálico) los electrones que deja el cinc son tomados por el (cobre)++ de la solución, las cargas negativas neutralizan a los positivos y se forma cobre metálico:
(cobre)++ + 2(electrones)- => cobre metálico
Y entonces si, los iones (cinc)++ que se habian formado pueden pasar a la solución. En resumen: un poco de cinc se disuelve y un poco de cobre se deposita.
Pero si logramos que esos electrones no pasen directamente del alambre a la solución sino que circulen por un cable externo, habremos armado una pila eléctrica.
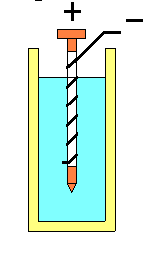 |
JABÒN CASERO
MATERIALES:
base para jabón
esencia cosmética
colorante cosmético
moldes
Pasos :
en una olla en baño maría vamos a poner la ase para jabón en pedazos
después de un tiempo veremos como se diluye , vamos a aumentar el
colorante y esencia lo ponemos con mucho cuidado en los moldes de tal manera
que después de una media hora al ambiente, se secara.
podemos sacar inmediatamente de los moldes, y tenemos nuestro jabón
sugerencias :
podemos incluir avena el la mezcla lo cual , hará un jabón exfoleante
viernes, 11 de enero de 2013
EXPERIMENTO SOBRE EFECTO JOULE

Vamos a realizar un experimento acerca de la electricidad, en donde veremos cómo encender fuego sin un encendedor o chispero. Éste es ideal para entender y explicar qué es lo que sucede en el efecto Joule.
Materiales:
* Papel
* Virulana o lana de hierro fina
* Batería de 9 Voltios
Procedimiento:
Como prometimos, este experimento de electricidad es muy sencillo. Primero coloca el papel sobre una superficie que no se queme. A continuación, pon la virulana sobre él, y envuélvelo como se muestra en el video. Para terminar, toca la virulana con los terminales de la batería y sopla un poco para “avivar” el fuego. Como veras, el papel se encenderá muy fácilmente.
viernes, 4 de enero de 2013
FLOTA... NO FLOTA"
MATERIAL:
1 probeta de 100 ml
25 ml de miel
25 ml de agua
25 ml de aceite comestible
25 ml de alcohol
Un pedazo de globo o popote, papel aluminio, cinta elástica y madera
PROCEDIMIENTO:
Vierta 25 ml de miel en una probeta de 100 ml, inclínela y añada con todo cuidado la misma
cantidad de agua. Hágala caer por las paredes de la probeta para que no se mezcle con la
miel. Enderece la probeta el vaso y verá que el agua flota sobre la miel porque es menos
densa que ésta.
Añada cantidades iguales de aceite y alcohol y obtendrá una columna de densidades formada
por cuatro líquidos superpuestos.
Si desea hacer este experimento más atractivo, añada algunos cuerpos sólidos. Tome primero
un pedacito de papel aluminio; haga una bolita, aplástela lo más posible y agréguela muy
suavemente en el alcohol. Verá como baja lentamente hasta detenerse en la miel.
Añada un pedacito de cinta elástica; llegará hasta el agua y allí permanecerá. Si agrega un
pedacito de globo o de popote de plástico llegará hasta el aceite, y un pedazo de madera
flotará en el alcohol.
Nota: Inténtelo con otros objetos pequeños y observe lo que pasa. Cuando los cuatro líquidos
son incoloros resulta interesante ver flotar diversos sólidos a diferentes alturas.
EXPLICACIÓN:
Todos los líquidos tienen una densidad; pero no de igual magnitud, los que son menos densos
permanecen por encima de otro y parece como si flotaran. Así se demuestra que la miel es
más densa que el agua y ésta que los dos líquidos que flotan sobre ella. A menor densidad
mayor flotación.
Mantequilla
Toma un litro de crema de leche , mejor si es de bolsa y la pones en refrigeración 1 hora antes, y la pones en una batidora , como si fueras a hacer Chantilly solo que no le pongas nada de azúcar o vainilla , depende de la batidora serán como 7 o 10 minutos veras como se va separando la grasa de el suero , puedes ir eliminando el suero para que no salpique mucho , cuando veas que tiene consistencia de mantequilla le agregas un poco de sal al gusto y tienes una mantequilla sencilla , le puedes agregar si quieres alguna hierba picada muy fina , por ej perejil , o albahaca , o ajo ,etc la metes en un molde o con una manga de pastelería haces besitos y la metes a refrigeración.
Mermelada de moras y frambuesas
 Ingredientes:
Ingredientes:
- 1,600 kr de moras
- 400 gr de frambuesas
- 1 Kg de azúcar
- Zumo de 1 limón
Preparación:1.- Lavamos y secamos las moras y las frambuesas. Las ponemos en un bol con el azúcar y dejamos macerar unas horas para que suelten todo su jugo.2.- Pasado el tiempo, ponemos todo en una cazuela alta y añadimos el zumo del limón. Cocemos a fuego lento, cuando empiece a hervir removeremos a menudo, hasta que la mezcla espese. Sobre unos 30-40 minutos. 3.- Pasamos la mermelada por un colador “chino” o pasapurés, para sacar las semillas si nos molestan.4.- Embotamos y esterilizamos los frascos para su conservación.
3.- Pasamos la mermelada por un colador “chino” o pasapurés, para sacar las semillas si nos molestan.4.- Embotamos y esterilizamos los frascos para su conservación. Trucos y Consejos:
Trucos y Consejos:
- Conservaremos la mermelada en tarros esterilizados previamente. Para ello debemos hervir las tapas y frascos durante 25 minutos y dejarlos secar sobre un paño limpio, de algodón, boca abajo(sin la tapa puesta). Llenamos los tarros hasta el borde superior, cerramos la tapa fuertemente(hasta que haga vacío) y ponemos al baño maría(el agua debe cubrir casi los botes por completo) durante 25 ó 30 minutos dependiendo del tamaño de los frascos. Apagamos el fuego, y dejamos enfriar las mermeladas dentro del agua. Una vez fríos todos los recipientes, los secamos, etiquetamos y guardamos en un lugar preservado de la luz hasta su consumo.
- Para que una mermelada asiente su sabor, esperaremos preferentemente dos semanas desde que se ha elaborado para consumirla.
- Para realizar tus mermeladas usa frutos maduros pero no estropeados.
- Esta mermelada está ajustada en azúcar para nuestro gusto. Si te gustan muy azucaradas echa la mitad de azúcar del peso de la fruta una vez limpia.
- Puedes aromatizar la mermelada con lo que más te guste: esencias, hierbas, licores…
Suscribirse a:
Entradas (Atom)









